La terapia génica en etapa clínica de Nanoscope Therapeutics, MCO-010, se centra en restaurar la visión de personas que padecen enfermedades degenerativas de la retina.
MCO-010 está actualmente en desarrollo y aún no está aprobado para uso en pacientes fuera de ensayos clínicos. Actualmente estamos colaborando con la Administración de Alimentos y Medicamentos de EE. UU. y la Agencia Europea de Medicamentos en el camino hacia la aprobación.
Si desea recibir actualizaciones futuras sobre el progreso de MCO-010, lo invitamos a unirse a nuestra lista de correo.

La necesidad insatisfecha abordada por la MCO-010
Las enfermedades degenerativas de la retina son afecciones devastadoras en las que las neuronas externas de la retina (fotorreceptores), las células sensibles a la luz del ojo, se deterioran progresivamente o mueren, lo que provoca una pérdida grave de la visión en los pacientes. Dado que los fotorreceptores no se regeneran, la pérdida de visión debido a estas afecciones es permanente. Hasta la fecha no se ha aprobado ningún tratamiento que restablezca la visión en estos pacientes.
Las distrofias retinianas hereditarias (IRD) son afecciones degenerativas de la retina hereditarias que se transmiten de padres a hijos. Las IRD son actualmente la principal causa de ceguera en la población en edad de trabajar. Hay cientos de mutaciones genéticas que se sabe que causan IRD.
La retinitis pigmentosa (RP) es un grupo de trastornos oculares hereditarios que afectan la retina. La RP es causada por mutaciones que se han encontrado en más de 100 genes diferentes, cada uno de los cuales contribuye al desarrollo y funcionamiento de la retina. La RP se caracteriza por la degeneración y disfunción progresiva de las células fotorreceptoras de conos y bastones de la retina, que son responsables de convertir la luz en señales eléctricas que el cerebro interpreta como visión. Inicialmente, afecta la visión periférica y conduce a la visión de túnel y, en una progresión posterior, afecta la visión central. La RP suele manifestarse durante la niñez o la adolescencia, pero también puede presentarse en la edad adulta. La RP produce una pérdida de visión permanente y progresiva hasta el punto de una ceguera profunda.
La enfermedad de Stargardt, también conocida como distrofia macular de Stargardt o degeneración macular juvenil, es un trastorno ocular hereditario que afecta la mácula en el centro de la retina. La mácula es responsable de la visión central nítida. La enfermedad de Stargardt generalmente se diagnostica durante la niñez o la adolescencia, aunque puede identificarse en la edad adulta.
Los síntomas de la enfermedad de Stargardt incluyen pérdida de la visión central, visión borrosa o distorsionada, dificultad para reconocer rostros, problemas de visión de los colores y un punto ciego en el campo visual central. Sin embargo, la visión periférica suele permanecer intacta. Lamentablemente, los pacientes con enfermedad de Stargardt avanzada llegan al mismo estado de pérdida profunda de la visión debido a la degradación de los fotorreceptores que los pacientes con RP.
La degeneración macular relacionada con la edad (DMAE) es una afección degenerativa de la retina que afecta a la población que envejece y es la principal causa general de ceguera retiniana. Independientemente de la forma (DMAE húmeda o seca), en la etapa final se produce atrofia geográfica (GA), en la que se degenera la retina externa.

Tecnología y diferenciación de nanoscopios.
La optogenética es un enfoque de terapia génica mediante el cual un gen exógeno que codifica proteínas sensibles a la luz (opsinas) se utiliza para funcionalizar las células para que se vuelvan sensibles a la luz.
Cuando los fotorreceptores degeneran, la mayoría de las demás neuronas de la retina sobreviven en los pacientes. Al hacer que las células retinianas supervivientes sean sensibles a la luz, la optogenética pretende permitir la generación de señales visuales en las neuronas retinales sensibilizadas a la opsina que se transmiten al cerebro a través del nervio óptico. Las terapias optogenéticas están diseñadas para funcionar independientemente de las mutaciones/causas genéticas subyacentes de la degeneración de la retina y no requieren la viabilidad del epitelio pigmentario/fotorreceptor de la retina, lo que ofrece la posibilidad de restaurar la visión incluso en las últimas etapas de la degeneración de la retina. enfermedades.
Dado que el mecanismo de acción de la terapia optogenética es diferente de la terapia génica clásica, se espera que la eficacia terapéutica sea independiente de las mutaciones subyacentes. Una limitación de los enfoques tradicionales de terapia génica es que solo pueden atacar mutaciones individuales y, en consecuencia, un pequeño subconjunto de pacientes con IRD son elegibles para el tratamiento. Además, en comparación con la terapia génica clásica, la terapia optogenética no requiere la presencia de fotorreceptores, por lo que también se puede aplicar a pacientes con pérdida grave de visión que carecen de fotorreceptores.
La opsina multicaracterística (MCO) es la opsina patentada y patentada de Nanoscope. MCO se compone de 3 componentes funcionales fusionados en un solo transgén. Estos componentes exhiben propiedades que son necesarias para una visión optogenética de alta calidad (alta sensibilidad a la luz, capacidad de respuesta en todo el espectro visible y cinética de respuesta a la luz rápida) cuando se expresan en las células diana. MCO es altamente sensible a la luz en todo el ancho de banda de color de la luz visual con una cinética rápida para minimizar el desenfoque, maximizando así la luz para permitir potencialmente una visión detallada y de alta calidad sin la necesidad de una amplificación de alta intensidad de las señales de luz ambiental para restaurar la visión del paciente.
MCO-010 (sonpiretigene isteparvovec) es una terapia génica patentada y protegida por virus adenoasociado tipo 2 (AAV2) que expresa MCO. MCO-010 está diseñado para transducir de manera eficiente e impartir sensibilidad a la luz funcional a las células bipolares en pacientes con una pérdida significativa de visión debido a la degradación de los fotorreceptores. MCO-010 se está evaluando para el tratamiento de la pérdida grave de visión en pacientes con retinitis pigmentosa y en pacientes con enfermedad de Stargardt.
MCO-010 se administra mediante una inyección intravítrea única en el consultorio, después de la cual las células bipolares de la retina expresan la proteína MCO, lo que las hace sensibles a la luz.
Las células bipolares existen más próximas a los fotorreceptores que a las células ganglionares de la retina (CGR). Como tal, apuntar a estas células tiene el potencial de preservar un mayor circuito de procesamiento visual. Además, a diferencia de las CGR, las células bipolares no tienen procesos de extensión lateral, lo que permite una activación más precisa. Además, hay aproximadamente diez veces más células bipolares que RGC, lo que ofrece la posibilidad de una mayor resolución espacial.
MCO ha sido diseñado de manera que cada uno de los tres componentes sensibles a la luz sea sensible a una porción diferente del espectro de luz visible. Así, cuando se expresa como una proteína de fusión, la sensibilidad a la luz se confiere a través de los diferentes colores de la luz visible.
Actualmente existen otros enfoques optogenéticos en distintas etapas de desarrollo preclínico y clínico. MCO es la única opsina optogenética que es de banda ancha (es decir, que responde a todo el espectro/colores de luz visual). MCO-010 se administra a las células de la retina mediante una inyección intravítrea única. Después de la inyección, la MCO expresada tiene una alta sensibilidad a la luz, una velocidad de respuesta rápida y es sensible en todo el espectro de luz visible y, por lo tanto, no requiere un dispositivo externo de estimulación/amplificación de luz intensa.
MCO-010 es la única plataforma optogenética que es rápida, sensible y sensible en todo el espectro visible, de manera independiente de mutaciones y enfermedades para tratar enfermedades degenerativas de la retina (RP y Stargardt).
No. Si bien muchos otros enfoques optogenéticos del desarrollo requieren amplificación de alta intensidad o dispositivos de estimulación externa, la MCO es sensible a la luz en todo el espectro de luz visible debido a sus múltiples componentes sensores de luz y no requiere estimulación lumínica de alta intensidad. El alto rango dinámico se logra gracias a las características únicas del sistema multicomponente detrás de MCO.
MCO-020 contiene una opsina MCO de próxima generación que se administra por vía intravítrea como ADN desnudo (sin envoltorio viral) que se administra a células diana específicas a través de una plataforma láser guiada por tomografía de coherencia óptica. MCO-020 se está desarrollando para el tratamiento de pacientes con pérdida grave de visión debido a la DMAE en etapa terminal.
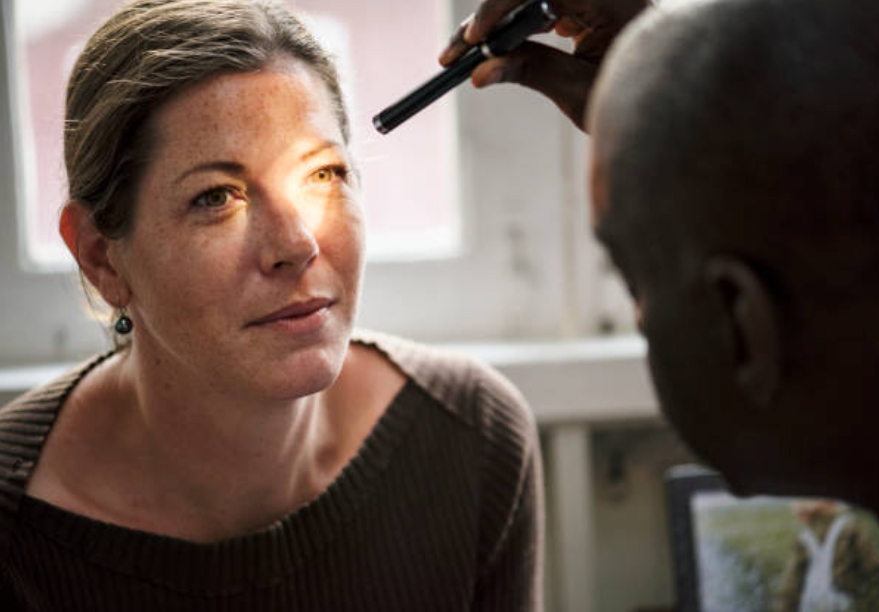
Perfil del paciente objetivo
MCO-010 está diseñado para pacientes con pérdida grave de visión relacionada con IRD, independientemente de la mutación. MCO-010 se está estudiando actualmente en pacientes con diagnóstico clínico de retinitis pigmentosa avanzada o enfermedad de Stargardt, independientemente de su mutación genética subyacente.
Aunque MCO-010 está diseñado para pacientes con enfermedad en etapa avanzada que presentan una pérdida de visión grave relacionada con IRD, es posible que los pacientes con pérdida de visión moderada también se beneficien. Actualmente estamos evaluando el camino para responder más completamente a esta pregunta.
No. El mecanismo de acción de MCO-010 es independiente de las mutaciones, ya que la sensibilidad a la luz introducida se imparte a las células bipolares en lugar de intentar reparar/hacer crecer los fotorreceptores a los que impactan los IRD. MCO-010 tiene el potencial de representar un tratamiento para todas las enfermedades retinianas hereditarias en etapa tardía.
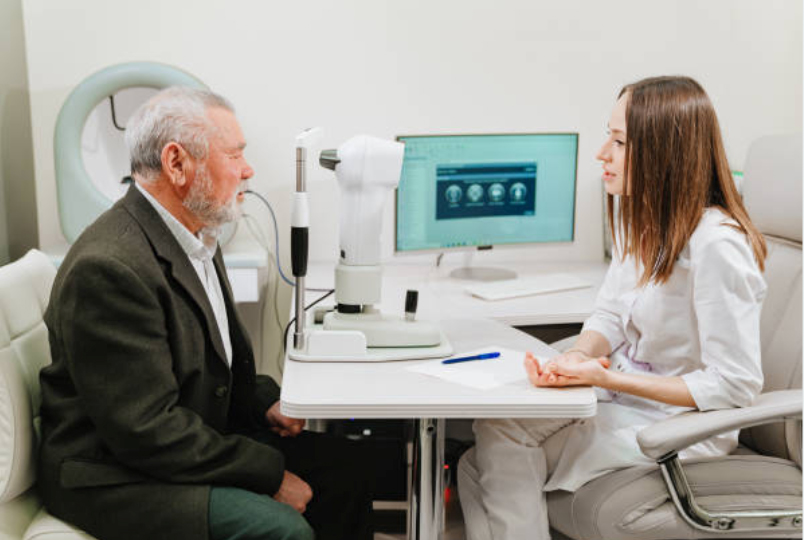
Ensayos clínicos y acceso a pacientes
Los ensayos de intervención para MCO-010 y MCO-020 en 2024 se encuentran en la fase de planificación y los actualizaremos aquí el próximo año.
Hay varios otros ensayos en los que los pacientes participan en un seguimiento continuo a largo plazo (LTFU) de los estudios originales. No aceptan nuevos pacientes para recibir tratamiento en estos estudios. Los detalles de estos estudios se pueden encontrar siguiendo los hipervínculos:
- Ensayo original de fase 1/2a en pacientes con RP en la India NCT04919473 y el estudio LTFU asociado NCT05921162.
- El ensayo clínico RESTORE Fase 2b, multicéntrico, aleatorizado, doble enmascarado y controlado de forma simulada (NCT04945772) LTFU se iniciará en breve.
- La compañía también iniciará un LTFU para el ensayo STARLIGHT de fase 2 de la terapia MCO-010 en pacientes Stargardt (NCT05417126).
Más información estará disponible aquí., https://nanostherapeutics.com/pipeline/clinical-trials/
MCO-010 está actualmente en desarrollo y aún no está aprobado para uso en pacientes fuera de ensayos clínicos. Actualmente estamos colaborando con la Administración de Alimentos y Medicamentos de EE. UU. y los reguladores europeos en el camino hacia la aprobación.
El costo de MCO-010 no se decide en esta etapa y la rentabilidad se determinará en el futuro a través de la investigación de resultados y economía de la salud.


